Hiđrocacbon là hợp chất hữu cơ quan trọng cấu tạo lên các chất trong thực phẩm, cơ thể sinh vật và con người. Vậy hiđrocacbon là gì? Có mấy loại hiđrocacbon và những đặc điểm của chúng như thế nào?… Hãy cùng VIETCHEM trả lời những câu hỏi này trong bài viết dưới đây.
I. Hiđrocacbon là chất gì?
1. Định nghĩa
Hiđrocacbon theo định nghĩa là một loại hợp chất hữu cơ mà trong cấu tạo chỉ bao gồm cacbon (C) và hidro (H). Chúng có thể liên kết với nhau bằng các liên kết đơn, đôi hoặc ba.
2. Phân loại hiđrocacbon
Dựa vào các liên kết các nguyên tử C và H mà Hiđrocacbon thường chia làm 3 loại như sau:
- Hiđrocacbon no: trong phân tử chỉ có liên kết đơn, gồm 2 nhóm chính là ankan và cycloankan.
- Hiđrocacbon không no: Trong phân tử có các liên kết đôi hoặc ba, gồm 3 nhóm chính anken (chứa 1 liên kết đôi), ankadien (chứa 2 liên kết đôi) và ankin (chứa 1 liên kết ba).
- Hiđrocacbon thơm: Các nguyên tử C khép kín tạo thành vòng.
Hợp chất Hidrocacbon là gì?
II. Tìm hiểu về Hiđrocacbon no
Chúng ta cùng tìm hiểu chi tiết hơn về các loại Hiđrocacbon khác nhau. Dưới đây là những đặc điểm nổi bật về Hiđrocacbon no.
1. Tìm hiểu về Ankan
Ankan là các hiđrocacbon không tạo mạch vòng, trong mỗi phân tử chứa số nguyên tử hydro cực đại và không chứa các liên kết đôi. Ankan còn có tên gọi khác là parafin.
– Công thức chung: ???2?+2(?≥1)
– Tên gọi:
- Tên thay thế: Số chỉ vị trí nhánh + tên nhánh + mạch nhánh chính + an
- Tên thông thường: Nếu chỉ có một nhánh duy nhất CH3 ở nguyên tử C số 2 thì thêm tiền tố iso, nếu có 2 nhánh CH3 ở C số 2 thì thêm tiền tố neo.
– Tính chất vật lý của Ankan
- Ở nhiệt độ thường, các ankan từ C1 đến C4 ở trạng thái khí; từ C5 đến C10 ở trạng thái lỏng; từ khoảng C10 trở lên ở trạng thái rắn.
- Nhiệt độ nóng chảy, nhiệt độ sôi và khối lượng riêng của Ankan nói chung đều tăng theo số lượng nguyên tử C trong phân tử tức là tăng theo phân tử khối. Ankan nhẹ hơn nước.
- Ankan không tan trong nước và đều là những chất không màu.
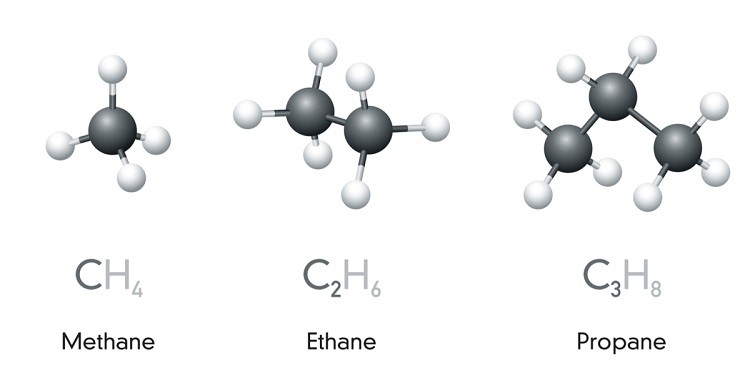
Một số hợp chất của ankan
– Tính chất hóa học của Ankan
- Phản ứng thế bởi Halogen:
Clo có thể thay thế lần lượt từng nguyên tử H trong phân tử metan. Chú ý: Sản phẩm thế ưu tiên với H ở C bậc cao.
CH4 + Cl2 → CH3Cl + HCl
CH3Cl + Cl2 → CH2Cl2 + HCl
CH2Cl2 + Cl2 → CHCl3 + HCl
CHCl3 + Cl2 → CCl4 + HCl
- Phản ứng tách.
Tách H2 (để hidro hóa)
Phản ứng cracking (bẻ gãy mạch cacbon)
- Phản ứng oxi hóa hoàn toàn (phản ứng cháy): CnH2n+2 + (3n+1)/2 O2 → n CO2 + (n+1)H2O
– Điều chế Ankan
Tùy theo điều kiện khác nhau mà ankan được điều chế từ các cách khác nhau như:
- Phòng thí nghiệm: CnH2n +H2 (Pt, Ni hoặc Pd), nhiệt độ -> CnH2n+2
- Trong công nghiệp, metan và các đồng đẳng được tách từ khí thiên nhiên và dầu mỏ.
– Chú ý:
- Phân biệt isoankan với isoankyl và neoankal với neoankyl.
- Isooctan là 2,2,4 – trimetylpentan.
– Ứng dụng: Hidrocacon có C1 đến C20 được ứng dụng làm nhiên liệu, điều chế chất sinh hàn. Nhờ tác dụng của nhiệt và các phản ứng oxi hóa không hoàn toàn tạo thành HCHO, rượu metylic, axit axetic,… Ngoài ra, nhiều ankan còn được dùng làm dung môi hữu cơ và dầu bôi trơn máy.
2. Tìm hiểu về Xicloankan
– Định nghĩa: Xicloankan là những hiđrocacbon no mạch vòng, chỉ chứa liên kết đơn trong phân tử.
– Công thức tổng quát: ???2?(?≥3).
Tên gọi của Xicloankan: Tên = số chỉ vị trí nhánh + tên nhánh + xiclo + tên mạch chính + an
– Tính chất hóa học:
- Phản ứng thế: Khi chiếu sáng hoặc đun nóng, nguyên tử hidro bị thay thế bởi nguyên tử halogen.
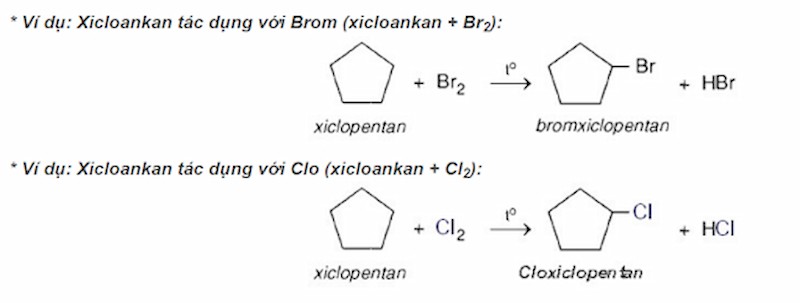
Phản ứng thế của Xicloankan
- Phản ứng cháy:
Phương trình tổng quát: ???2?+(3?/2)?2→???2+??2?⇒???2+??2?
- Phản ứng cộng
Ngoài phản ứng trên, Xiclopropan, Xiclobutan còn có phản ứng cộng mở vòng. Riêng Xiclopropan còn phản ứng với dd brom hoặc axit:
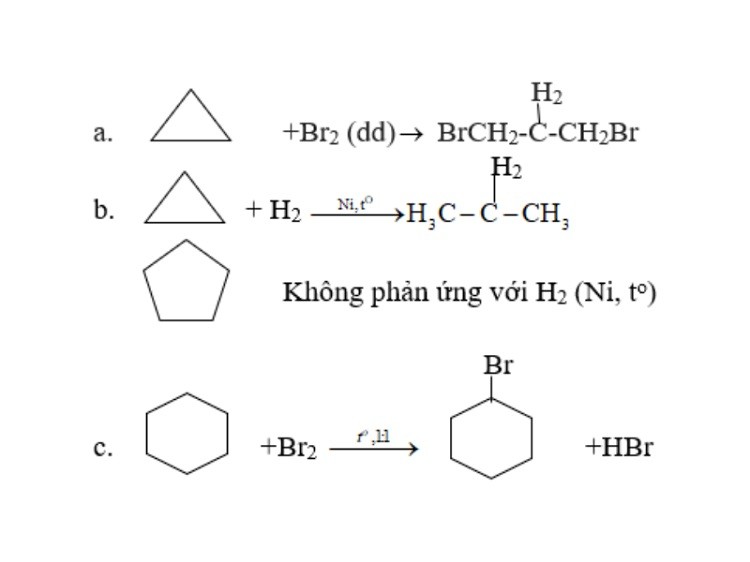
Phản ứng cộng mở vòng của Xicloankan
– Điều chế Xicloankan:
Xicloankan được điều chế bằng phương pháp chưng cất dầu mỏ, khí tự nhiên chưng cất phân đoạn.
Ngoài ra, nó còn có thể điều chế bằng cách H2, đóng vòng ankan.
III. Tổng quan về Hiđrocacbon không no
Hiđrocacbon không no theo định nghĩa chính là hiđrocacbon có chứa ít nhất một liên kết đôi trở lên trong cấu trúc phân tử của nó, tuy nhiên trong phân tử phải không cómạch vòng như hiđrocacbon thơm, mà chỉ có dạng mạch thẳng hoặc phân nhánh.
1. Phân loại Hiđrocacbon không no
Hiđrocacbon không no được phân loại thành 3 nhóm chính dưới đây:
- Anken: CnH2n với n≥2.
- Ankadien: CnH2n-2 với n≥3, trong phân tử có hai liên kết đôi.
- Ankin: CnH2n-2 với n≥2, trong phân tử có một liên kết ba.
- Dạng hỗn hợp của ba dạng trên.
Ngoài ra, một số Hiđrocacbon không no có chứa liên kết đôi, chúng còn chia thành những đồng phân cis-trans (đồng phân hình học) do những nhóm này mỗi một bên của liên kết đôi khác nhau. Chính vì vậy mà khi quay quanh mặt phẳng chứa liên kết đôi thì trở thành các dạng khác nhau.
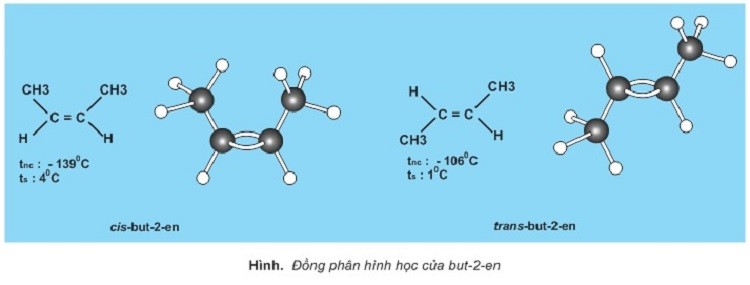
Đồng phân hình học của but-2-en
2. Tính chất hóa học của Hiđrocacbon không no
Những phản ứng đặc trưng của Hiđrocacbon không no gồm:
- Phản ứng với hidro tạo ra hiđrocacbon no (nếu hidro hóa hoàn toàn):
H2+C3H6→C3H8
2H2+C3H4→C3H8
- Phản ứng oxi hóa gồm các phản ứng cháy, anđehit hóa, rượu hóa,…
- Phản ứng với hidro clorua tạo ra các chất dẫn xuất halogen như:
HCl+C3H6→C3H7Cl
CH≡CH+HCl→CH2=CHCl
- Phản ứng cháy của Anken: CnH2n+(3n2)O2→nCO2+nH2O
- Phản ứng cháy của ankadien và ankin: CnH2n-2+((3n-1)/2)O2→nCO2+(n-1)H2O
IV. Tổng quan về Hiđrocacbon thơm
Hiđrocacbon thơm là Hiđrocacbon mà phân tử của nó gồm các nguyên tử cacbon khép kín.
1. Phân loại hidrocacbon thơm
Chúng bao gồm:
- Benzen và đồng đẳng của nó: Benzen C6H6 và các hiđrocacbon thơm khác như C6H6, C8H10… Chúng lập thành dãy đồng đẳng có công thức phân tử chung ???2?−6 (?≥6).
- Hiđrocacbon thơm có nhiều nhân: Cấu trúc phức tạp hơn, nhiều vòng benzen trong phân tử.
- Hợp chất thơm không chứa vòng benzen: Chứa những vòng khác không phải benzen.
2. Tính chất hóa học của hiđrocacbon thơm
Những phản ứng đặc trưng của Hiđrocacbon thơm:
- Phản ứng thế nguyên tử H của vòng Benzen.
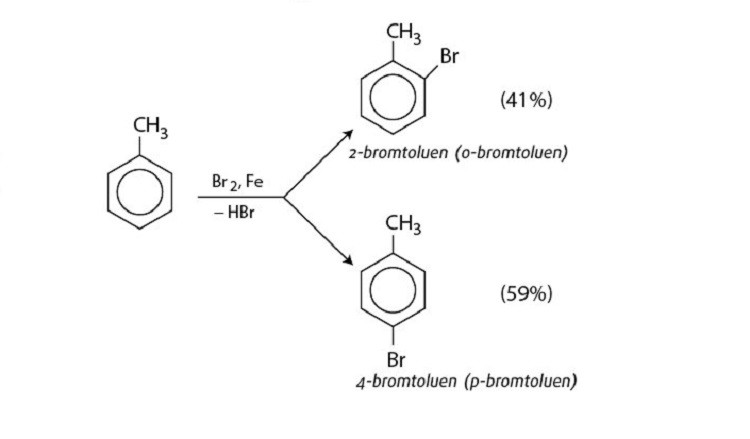
Phản ứng của benzen với halogen
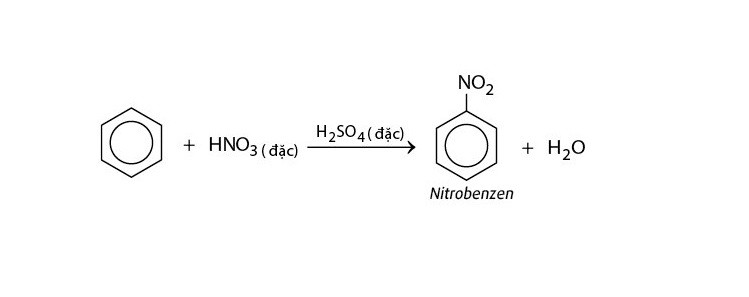
Benzen tác dụng với axit nitric
- Phản ứng cộng:
- Phản ứng oxi hóa không hoàn toàn:
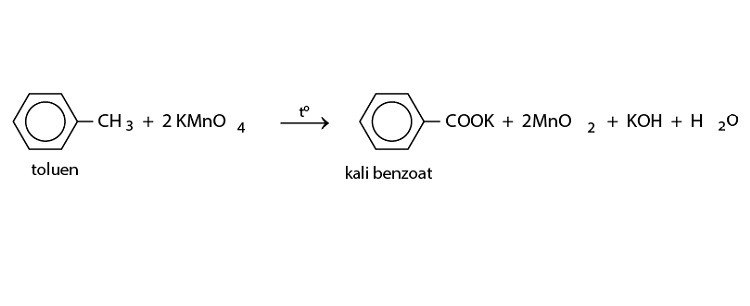
Phản ứng Toluen với KMnO4
- Phản ứng cháy: ???2?−6+(3?−32)?2→???2+(?−3)?2?
Hiđrocacbon thơm, đặc biệt là Benzen và toluen là những nguyên liệu rất quan trọng được sử dụng nhiều trong công nghiệp hóa học. Việc sản xuất benzen, toluen hiện nay chủ yếu vẫn từ nhựa và than đá hoặc từ sản phẩm đề hidro đóng vòng hexan, heptan tương ứng.
Trên đây là những thông tin cơ bản về Hiđrocacbon. Nếu có bất cứ thắc mắc nào bạn có thể liên hệ với chúng tôi trong thanh chat phía cuối màn hình hoặc tham khảo thêm những bài viết trên vietchem.com.vn.
